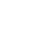ISO 13485认证只是门槛?深析医疗设备零件加工中的“全生命周期可追溯”生死线
更新时间:2026-02-27
在2026年的全球医疗器械监管版图中,合规已不再仅仅是一纸证书那么简单。随着中国NMPA、美国FDA以及欧盟MDR对医疗器械安全监管力度的空前加强,医疗设备零件加工行业正面临着一场从“结果合格”向“过程绝对可控”的深刻变革。 许多企业误以为拿到了ISO 13485质量管理体系认证就拥有了通往市场的通行证,然而现实数据表明,因缺乏完善的追溯体系而导致的产品召回事件,在过去一年中仍占据了医疗器械不良事件的显著比例。本文将深入剖析为何“全生命周期可追溯”已成为医疗设备零件加工企业的生死线,以及如何构建这一核心竞争力。

从“合规底线”到“生存红线”:追溯体系的战略升级
过去,医疗设备零件加工企业的关注点往往集中在最终产品的尺寸精度和表面光洁度上,认为只要成品检验合格即可交付。但在当前的监管环境下,这种思维模式极具风险。监管机构不仅要求产品本身符合标准,更要求企业能够瞬间还原产品从原材料入库、切削加工、表面处理、清洗包装到最终发货的每一个环节数据。
一旦市场上出现不良反馈,若企业无法在24小时内提供该批次零件的完整“数字档案”,包括原材料炉号、加工机台参数、操作人员记录、环境温湿度数据等,将面临巨额罚款甚至吊销生产许可的风险。因此,建立一套严密的追溯体系,不再是应付检查的“加分项”,而是决定企业生死的“红线”。对于从事高精密医疗设备零件加工的企业而言,追溯能力直接等同于市场准入资格。
破解数据孤岛:构建全流程数字化追溯链条
实现全生命周期可追溯的最大挑战,在于打破生产过程中的“数据孤岛”。在传统的医疗设备零件加工车间,设计图纸在PLM系统中,加工工艺在CAM软件里,实际加工数据在CNC机床控制器内,而质检报告则躺在纸质单据或独立的Excel表格中。这种碎片化的信息管理模式,使得追溯工作如同大海捞针。
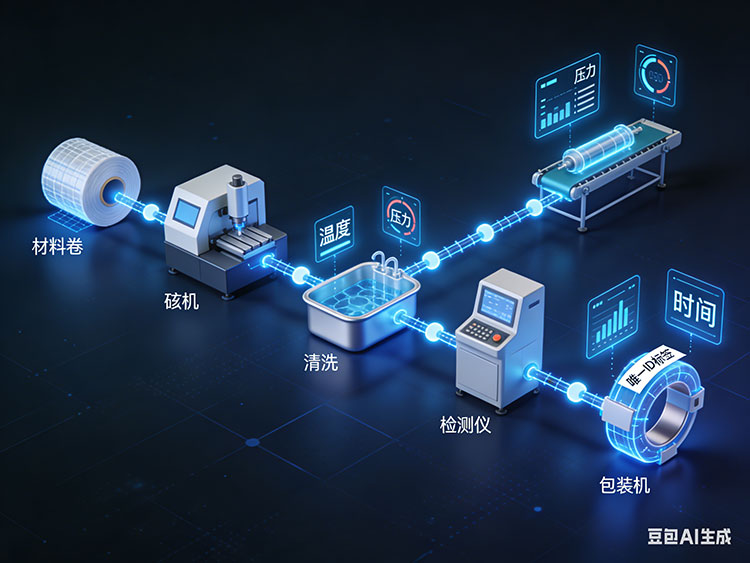
材料溯源与工艺验证:确保微观层面的绝对安全
医疗植入物和手术器械对材料的生物相容性和机械性能有着近乎苛刻的要求。在医疗设备零件加工领域,材料溯源是追溯体系中最基础也最关键的一环。企业必须确保每一克钛合金、PEEK材料或不锈钢,都能追溯到上游钢厂的具体炉号和质保书(MTR)。任何材料的混用或来源不明,都可能导致灾难性的临床后果。

未来展望:AI赋能下的智能追溯新范式
展望2026年及未来,医疗设备零件加工的追溯体系将不再局限于被动记录,而是向主动预测和智能预警演进。借助人工智能和大数据分析技术,追溯系统可以实时分析海量生产数据,提前识别出可能导致质量偏差的异常趋势。例如,当系统检测到某台机床的振动频谱出现微小变化,虽未超出公差范围,但AI算法可预测其在未来几小时内加工出的零件可能存在微裂纹风险,从而自动触发停机维护指令,并锁定相关半成品进行复检。
这种智能化的追溯模式,将把质量控制从“事后补救”彻底转变为“事前预防”。对于医疗设备零件加工行业而言,这不仅是技术的迭代,更是质量管理哲学的升华。只有那些能够率先构建起智能化、全生命周期可追溯体系的企业,才能在日益严苛的全球竞争中立于不败之地,真正守住那条关乎生命与责任的生死线。
在医疗器械这个容错率为零的行业,医疗设备零件加工不仅仅是金属与刀具的物理碰撞,更是数据与责任的严密编织。ISO 13485认证只是入场券,唯有构建起无死角的全生命周期可追溯体系,企业方能行稳致远,为全球医疗健康事业提供坚实可靠的支撑。